Oftalmopatia de Graves
O que é Oftalmopatia de Graves?
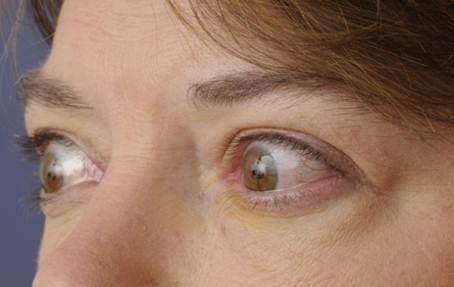
É a alteração da órbita provocada por uma doença da glândula tireóide, na maioria das vezes o hipertireoidismo.Como a órbita é uma caixa óssea que não se distende, esse aumento do músculo e/ou da gordura provoca o deslocamento do globo ocular para fora. Esta afecção foi descrita primeiramente por Robert Graves, no ano de 1835.
Causas

Sintomas

Tratamento

